引言
我国约有1.4亿糖尿病患者,其中1型糖尿病多发于儿童青少年,需终身注射胰岛素,并发症风险高。传统胰岛移植供体极度匮乏,全球仅数千例。2026年2月,中国团队在《柳叶刀·糖尿病与内分泌学》发表突破性研究:利用干细胞再生胰岛微创移植,成功重建1型糖尿病患者胰岛功能,实现血糖自主调控。
技术突破:内胚层干细胞体系
团队建立内胚层干细胞技术体系,仅需2步分化、14天规模化制备“再生胰岛组织”。相比传统多能干细胞路径(10步、40天以上、成瘤风险高),新体系效率提升3倍,且细胞定向分化、体内不增殖,安全性显著提高。仅需健康捐献者5毫升血液,即可构建供数百万人使用的干细胞“种子库”。
临床进展
研究治疗三例严重1型糖尿病患者,均取得积极效果:
病例1(30岁女性,病程18年):自体内胚层干细胞移植配合标准免疫抑制。术后胰岛功能恢复,胰岛素用量减少85%。但患者自行停用免疫抑制剂后,移植功能丧失——证明即便自体细胞也需免疫抑制保护。
病例2(45岁男性,爆发性1型糖尿病):异体内胚层干细胞移植配合标准免疫抑制。术后36周完全脱离胰岛素,血糖平稳维持超过26个月,实现“功能性治愈”。
病例3(15岁女性,脆性1型糖尿病):异体移植后血糖稳定性显著提升,严重低血糖事件消失,生活质量大幅改善。
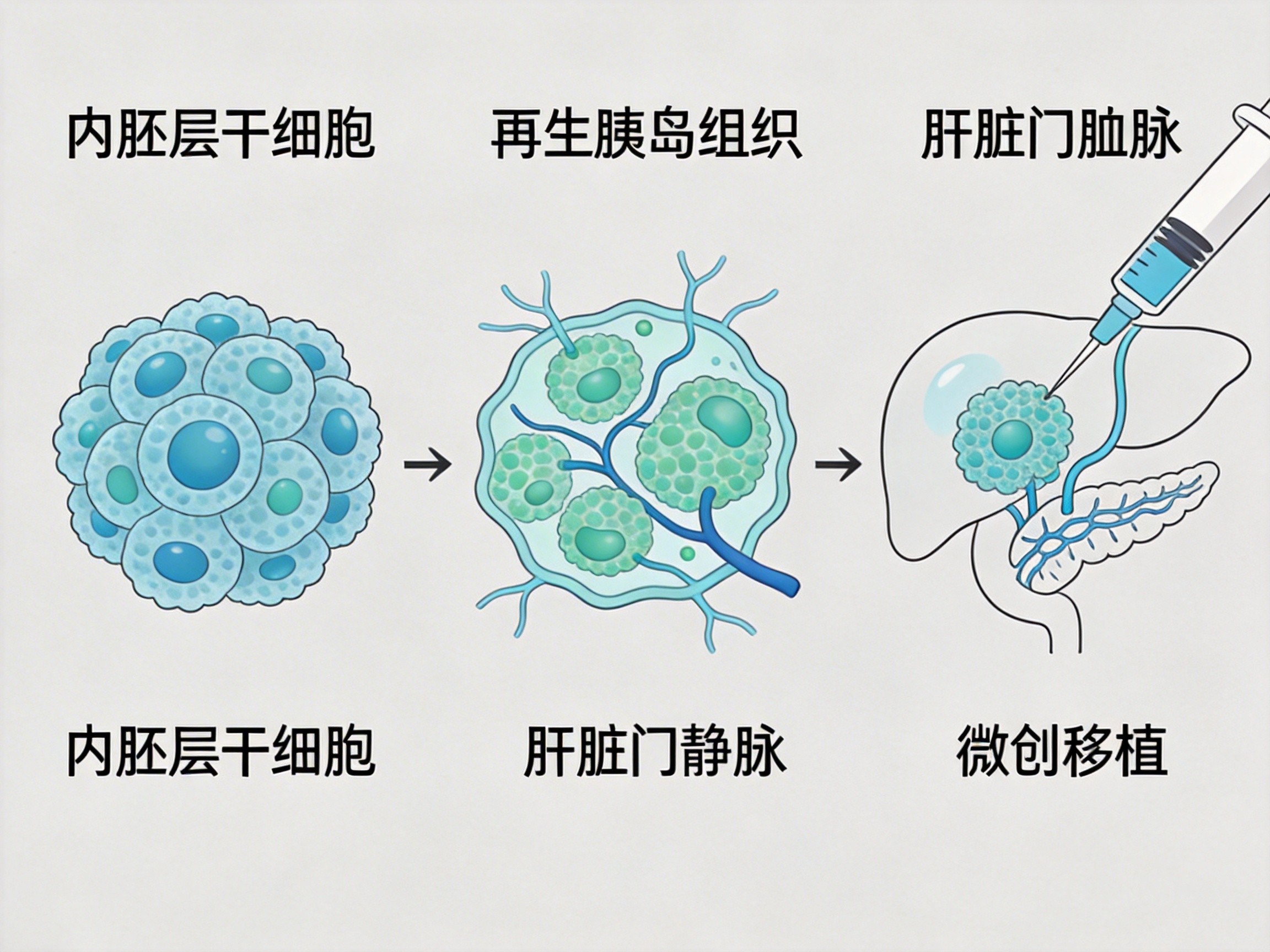
微创移植
移植过程简便微创:局部麻醉下,经皮肝门静脉穿刺,将指尖大小的再生胰岛组织注入肝脏,全程不到30分钟。移植物在肝脏中“落户”,实时感知血糖变化,精准分泌胰岛素,相当于植入“智能血糖调节器”。
当前局限与未来展望
挑战
- 需长期免疫抑制,存在感染等风险
- 尚处临床试验阶段,未大规模普及
- 主要针对1型糖尿病,2型应用在探索
未来方向
团队正研发: - 通用型+免疫逃逸再生胰岛:基因编辑实现无免疫抑制治疗 - 安全元件内置:可调控“开关”确保长期安全
基于该技术的“异体人再生胰岛注射液”已获中、美新药临床试验批件,成为全球唯一同时获批中美的再生胰岛药物。预计最早2029年有望惠及患者。
对基层医生与患者的启示
基层医生
- 了解前沿进展,未来可能成为重要治疗选项
- 识别适宜患者(1型、胰岛功能严重衰竭、频发低血糖)
- 客观介绍优势与局限,管理患者期望
患者
- 理性看待突破,尚未成为常规治疗
- 通过合规医疗机构进行,警惕商业炒作
- 坚持现有规范治疗,预防并发症
结语
干细胞再生胰岛技术标志着糖尿病治疗从“终身控糖”向“功能性治愈”的跨越。对中国1.4亿糖尿病患者而言,这意味着“告别胰岛素”的希望之光已被点亮。基层医生与患者应紧跟科技前沿,保持理性期待,共同迎接糖尿病治疗的新时代。
(本文基于2026年2月27日发表于《柳叶刀·糖尿病与内分泌学》的临床研究整理,仅供参考。)